We must explain to you how all seds this mistakens idea off denouncing pleasures and praising pain was born and I will give you a completed accounts of the system and expound.
123/A, Miranda City Likaoli Prikano, Dope United States
+0989 7876 9865 9
info@example.com
Özel geliştirilmiş Sanakin® Teknolojisi sayesinde, hastanın kanından elde edilen otolog, Otolog Sitokin Zengin Serum (ACRS) elde edilir. Yüksek tolere edilebilirliği sağlamak için, hiçbir suni katkı maddesi kullanılmamaktadır. Bu serum ile vücuttaki her türlü enflamasyon tamamen otolog şekilde tedavi edilebilir. Teknolojinin bir diğer avantajı ise kişinin kendi rejenerasyon güçlerinin etkinleştirilmesidir. Buradaki odak noktası pozitif interlökin ve büyüme faktörlerinin elde edilmesidir, bunlar enflamasyon sürecine etkili biçimde müdahale eder, durdurur ve ardından rejenerasyonu tetikler.
SANAKİN® yardımıyla yapılacak bir tedavinin sayısız avantajı vardır:
• Son derece doğal bir yöntemdir ve diğer tedavi yöntemleriyle karşılaştırıldığnda güvenirliği tartışılmaz.
• Vücudun kendi rejenerasyon güçlerini destekler.
• Yan etkisiz tedavi şansı ile aşırı doz olasılığı ortadan kalkmaktadır.
• Yaşam kalitesinin iyileştirilmesini sağlar.
• Her endikasyon için karmaşık olmayan kullanım şekli ile tedavinin kolayca uygulanması mümkündür.
• Hızlı uygulama imkânı ile hasta konforu benzersizdir.
• Doktor tarafından kişiye özel tedavi seçeneği geliştirilebilir.
Sayfanın diğer bölümlerinde SANAKİN® kullanımının temelini açıklayan kapsamlı bir genel bakış bulabilmektesiniz.
Bu bölümlerde çeşitli endikasyonlarda SANAKİN® kullanımına da değinilmiştir.
Sitokin ağı
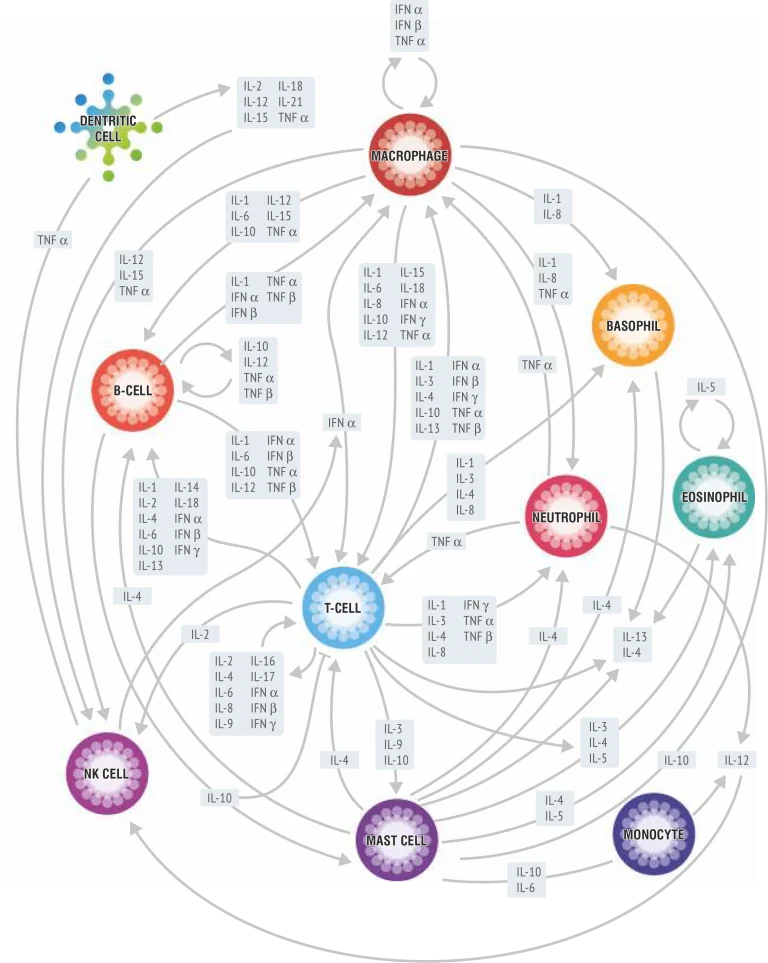
Sitokinlerin incelenmesine yönelik ilk çalışmalar, bağışıklık sistemi ve kan hücrelerinin biyolojik süreçlerinin anlaşılabilmesi için yapılan çalışmaların ayrılmaz bir parçasıdır.
Bağışıklık sistemi vücut sağlığına zarar verecek her türlü etmene karşı hızlı ve güçlü yanıtlar oluşturur. Bu son derece etkili yanıt süreci, immün sistemde görev yapan hücrelerin yanı sıra, bağışıklık hücreleri arasında sinyal iletiminde görev alan, aynı zamanda organizmanın diğer sistemlerinde de birçok olaya müdahale eden protein grubu sayesinde gerçekleşir. Örneğin, sitokinler (lenfokin veya interlökin olarak da adlandırılırlar) beynimizdeki sıcaklık merkezlerini kontrol ederken diğer yandan, iltihaba yanıt veren maddeleri de ak ve ederler ve sinir sistemine mesaj gönderen haberci molekülleri de tetiklerler.
Sitokin molekül ailesi, neredeyse insan vücudunun her yerinde aktif olan, şaşırtıcı derecede yüksek sayıda üyeden oluşur. Spesifik hücreler tarafından oluşturulurlar ve bu hücrelerin çevrelerine salınırlar. Salındıkları doku lokasyonlarında, ya kısmen engelleyici ya da kısmen uyarıcı etkiler sağlayarak, komşu hücreler arasındaki etkileşimleri düzenlerler. Bu açıdan, hormonlarla karşılaştırılırlarsa, hormonların sinyal iletimini vücudumuzda çok daha uzun mesafede bulunan dokularda gerçekleştirdikleri düşünülmelidir. Ayrıca sitokinler, farklı hücreler tarafından oluşturulabilir ve birçok farklı dokuda etkilerini gösterebilir.
İnsan organizmasının hır tür zararlı etkene karşı iki p savunma mekanizması vardır. Bağışıklık yanıtu, hücresel tip ve humoral tip olmak üzere iki bölümden oluşur. Hücresel immünitenin temel yapı taşları; lenfosit, monosit, makrofaj, doğal öldürücü (natural killer) hücreler, antijen sunan hücreler vb. olup, humoral immünitenin asil üyeleri ise immün globülinlerdir.
Sitokinler:
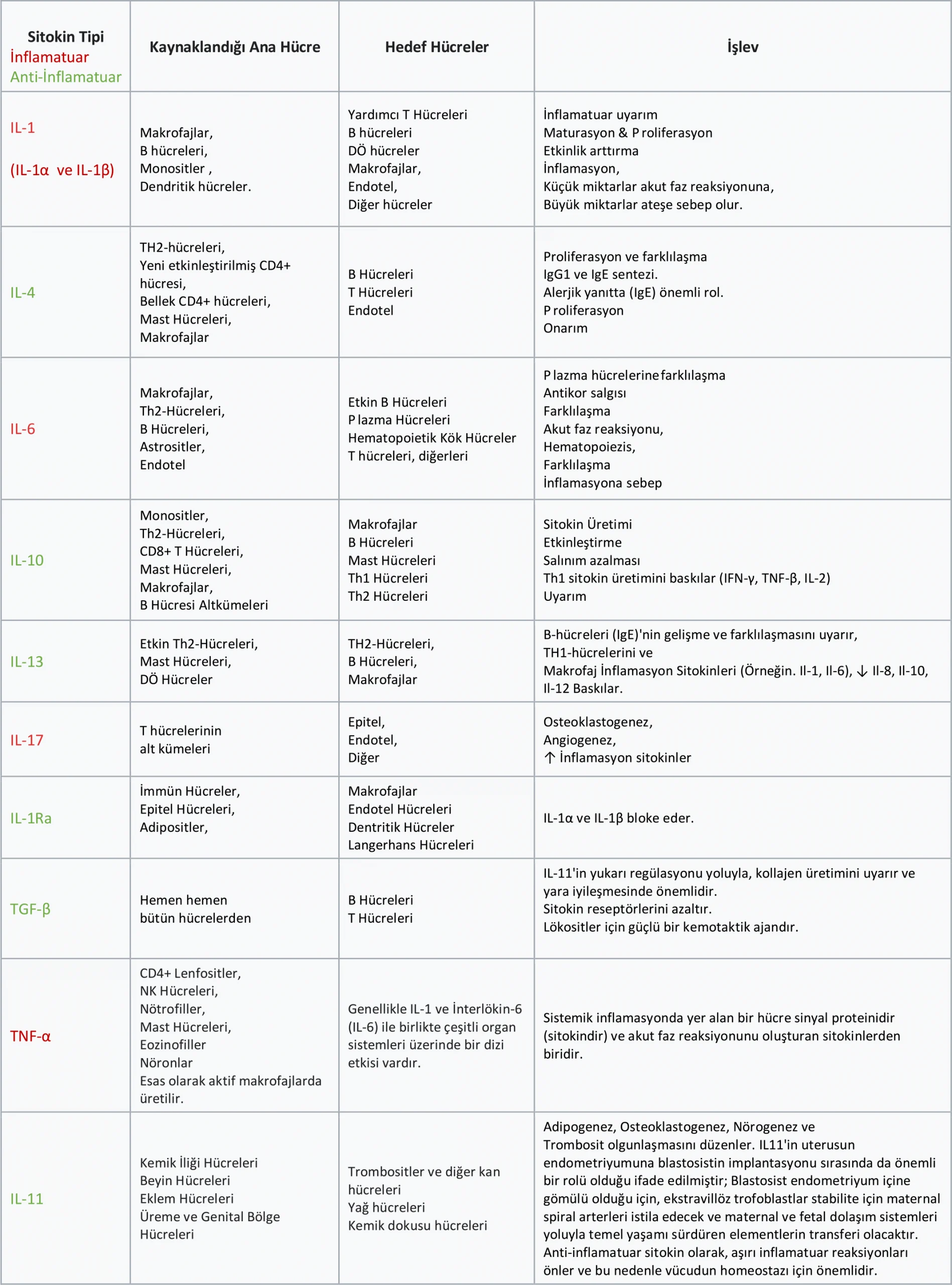
Tablo 1: Sitokin ağı üyelerinden örnekler.
Hücre biyolojisi büyüme faktörlerini, bir hücreden diğer bir hücreye sinyal ileten ve böylece bilgi taşıyan proteinler olarak tanımlar. Ayrıca, “sinyal proteinleri” olarak çok çeşitli hücre içi süreçleri düzenlerler ve özellikle çok hücreli organizmaların gelişiminde rol oynarlar.
Büyüme faktörleri – kısaca GF – hücre proliferasyonu ve/veya öncü hücrelerin (progenitör hücreler) veya kök hücrelerin somatik hücrelere farklılaşmasında
etkisi olan proteinlerdir.
Al büyük büyüme faktörü ailesi vardır:
• FGF ailesi (Fibroblast Büyüme Faktörü)
• TGF ailesi (Dönüştürücü Büyüme Faktörü)
• Hedgehog
• Wingless
• Delta and Serrate
• Ephrine
Büyüme faktörleri ya salgılanır – yani hücreler tarafından çevrelerine verilir – ya da membran kararlıdırlar. Membran-kararlı büyüme faktörleri hedef hücrenin reseptörleri tarafından algılandıkları zaman etkilerini göstermeye başlarlar. Sadece ilgili büyüme için spesifik reseptörü taşıyan hücreler faktör (ligand)
sinyale tepki verebilir. Ligandına bağlandığında, reseptör – hücre içindeki konformasyon değişikliği ile – daha fazla sinyal yoluyla sonuçlanan bir sinyal
üretir. Bunun sonucunda genlerin aktivasyonu veya deaktivasyonu gerçekleştirilir.
Farklı sinyal indüksiyonlarına sahip çok sayıda büyüme faktörü de bilinmektedir. Örneklenecek olursa:
• Fibroblast Büyüme Faktörü (FGF)
• Dönüştürücü Büyüme Faktörü (TGF)
• Trombosit Türevli Büyüme Faktörü (PDGF)
• Epidermal Büyüme Faktörü (EGF)
• Granülosit-Makrofaj Koloni Uyarıcı Faktörü (GMCSF)
• Vasküler Endotel Büyüme Faktörü (VEGF)
• İnsülin benzeri Büyüme Faktörleri (IGF)
• Hepatosit Büyüme Faktörü (HGF)
• İnterlökin-1 beta, -8 (IL-1 beta, IL-8)
• Sinir Büyüme Faktörü (NGF)
• Hematopoek Büyüme Faktörleri: Eritropoien ve Koloni Uyarıcı Faktörler,
örneğin G-CSF
Peptidler biyokimyasal araştırmaların ilgi odaklarındandır çünkü birçoğu insan vücudundaki düzenleyici işlevleri gerçekleştirmektedir. Büyüme faktörleri, aynı zamanda genç organizmaların gelişimini kontrol eden ve ilerleyen yaşam döngüsünde, iyileşme süreçleri ve onarım mekanizmalarından sorumlu olacak
olan maddelerdir.
Büyüme faktörleri, farklı uyaranlar tarafından oluşturulur, uyarılır veya dağılır. Reseptörleri ile olan etkileşimleri hücrelerde basamaklı sinyal etkileşimlerini tetikler ve bunun sonucunda genlerin akvitelerini seçici olarak regüle ederler.
Fibroblast büyüme faktörü; vaskülarizasyonu, kolajen sentezini, yara kontraksiyonunu, matriks sentezini ve epitelizasyonu smüle eder.
FGF reseptörleri, dış hücre zarlarında yüzeyel olarak bulunmaktadırlar ve FGF bağlandıktan sonra sinyaller hücrenin içine ilerler. Bu tarz reseptörlere transmembran reseptörler de denir. Hücre bölünmesine, farklılaşmasına veya göçüne neden olurlar.
FGF-1 bu ailenin en belirgin temsilcisidir. FGF-1 sadece fibroblastların proliferasyonundan sorumlu değildir aynı zamanda kolajen sentezinden de sorumludur. En önemlisi, kan damarlarının iç yüzeyini kaplayan endotel hücrelerinde de bulunmalarıdır. Yeni damar oluşumu – anjiyogenez üzerinde çok önemli bir etkisi bulunur. Bu süreç, yara iyileşmesi ve doku onarımı için oldukça önemlidir.
Keratinositlerin yarayı kapladığı ve epitelizasyonu oluşturduğu yara iyileşmesi döneminde görev alır.
TGF sitokin ailesine dâhildir. Sitokinler ayrıca farklılaşma, büyüme ve bağışıklık reaksiyonları gibi hücre fonksiyonlarını da düzenler ve uyarır. TGF, sırayla birkaç alt aileden oluşur. Örneğin, TGF-α, tümör hücreleri tarafından ürelirken, TGF-β, yara iyileşmesinde rol oynar.
TGF-β (Dönüştürücü Büyüme Faktörü β)
• Yara izinin alanını, derinliğini azalr.
• Korkoidlerin neden olduğu yara iyileşme bozukluklarını tersine çevirir.
• Fibroblastların çoğalmalarını destekler.
• Kolajen sentezini uyarır.
• Monositler tarafından FGF ve PDGF salgılanmasını teşvik eder.
TGF-α (Dönüştürücü Büyüme Faktörü α)
• Mezenkimal, epitelyal ve endotelyal hücreleri uyarır.
IGF-1, kanser gelişimi, hücre proliferasyonu ve apoptozun inhibisyonu ile bağlantılı bu grubun bir temsilcisidir.
HGF, fibroblastlar tarafından kolajen sentezini arrır ve yara iyileşmesinde hücre bölünmesini hızlandırır.
MSH’ ler, çeşitli biyolojik süreçleri kontrol eden sinyal molekülleridir. Örneğin, α -melanosit uyarıcı hormon (α-MSH), pigmentlerin gelişimini indükler.
PDGF, kan trombositleri tarafından salınan çeşitli faktörlere bölünür. Yara iyileşmesi ve fibroblastların bölünmesinde görev almaktadır. Özellikle embriyonik dönemde daha yoğun olarak bulunurlar.
• Kolajen sentezini, vaskülarizasyonu ve fibroblast bölünmesini uyarır.
• Makrofajları ve nötrofilleri aktive eder.
• β -TGF’yi etkinleştirir.
• Kök hücrelerin dokuya ulaşmasını sağlar.
Yine bu grubun bir parçası olan G-CSF ve M-CSF faktörleri gibi, GM-CSF’ de fagositler arasında sayılan nötrofilik granülositlerin ve makrofajların gelişiminden sorumludur.

Vücudun kendi sinyal proteinleri arasındaki dengesizlik, zarar verici
interlökin-1 artışına , doku hasarlarına, ağrıya, enflamasyona ve ödeme yol açar. İnterlökin-1’in doğal antagonist ise interlökin-1 reseptör antagonistdir.
Sanakin® yardımıyla elde edilmiş vücudun kendi serumu, hastanın kendi kanından elde edilmiş daha yüksek konsantrasyonlu doğal antagonist ve aynı zamanda önemli büyüme faktörlerini içerir. An enflamatuar sitokin ilgili reseptöre bağlanır. Böylece zarar verici sitokinin dokuda bulunan hücre alanlarına erişmesine engel olunur.

Doğal antagonist sitokinler belirgin bir enflamasyon önleme etkisine sahiptir ve büyüme faktörleri ile birlikte hasarlı dokunun rejenerasyonunu destekler. Denge yeniden sağlanır, böylelikle enflamasyon geriler.
Hedef
Sanakin® tıbbi ürün kullanımı ile sitokinlerin, otolog serum içeriğinde artan konsantrasyondaki varlığının tespiti hedeflenmişr. Bu sayede doktorlara, enflamasyon nedenli hastalıkların tedavisinde, otolog serum kullanımı ile etkin şekilde tedavi etme imkanı sağlanır. 1–3 saatlik inkübasyon sonrasında, serum içerisindeki enflamasyonu önleyici sitokinlerin kantitatif ölçümünün daha fazla olmasıyla birlikte aynı zamanda enflamasyonu tetikleyen sitokinlerin değerlerinde de düşüş tespit edilmiştir.
Metod
• 4 hastadan 40 ml otolog venöz kan alınmasını takiben:
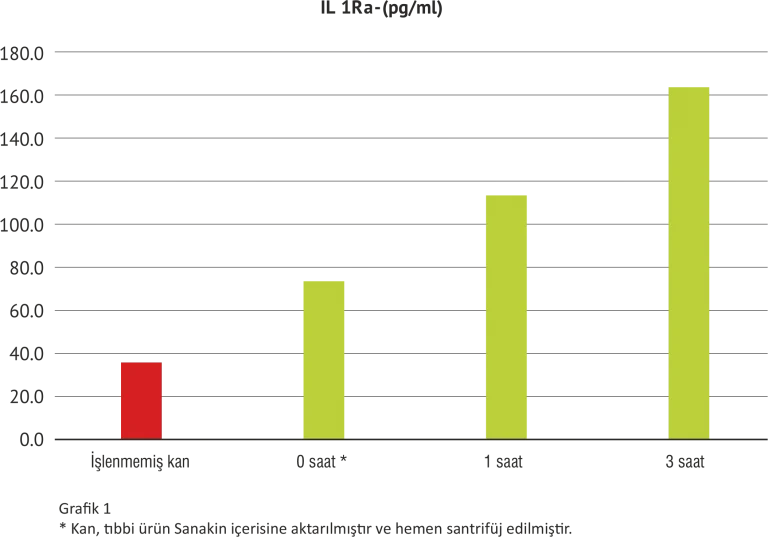
Grafiksel değerlendirme ve açıklama (Grafik 1)
İşlenmemiş Kan: İnkübasyona tabii tutulmayan ve Sanakin® tıbbi cihaz kitinin içine konulmamış kan, venöz kan alımında kullanılan kan alma tüpü ile hemen
santrifüj edilmiştir.
1. 1–3 saatlik inkübasyon sonrasında oluşan serumun içerisinde yüksek konsantrasyonda enflamasyonu tekleyici sitokinin bulunmadığı ispat edilebilmiştir.
2. Ayrıca, inflamasyonu önleyici sitokin IL-1Ra, 1 saat sonra 3 kat ve 3 saat sonra da 4,5 kat daha fazla konsantrasyonda elde edilebilmiştir.
• İnterlökin-1 Reseptör Antagonis (IL-1Ra), vücua İnterlökin-1 (IL-1) için doğal önleyici molekül olarak ortaya çıkar ve İnterlökin-1 (IL-1) tarafından tetiklenen enflamasyon süreçlerinin regülasyonunda önemli bir rol oynar.
• Etkisi, İnterlökin-1 (IL-1)’in etkisini durdurmaya dayanır ve bu etkiyi de İnterlökin-1 (IL-1) yerine hedef hücrede İnterlökin Reseptörüne bağlanmasıyla ve bu sayede İnterlökin-1 (IL-1)’in bağlanmasını bloke etmesiyle gerçekleştirir.
Grafiksel değerlendirme ve açıklama (Grafik 3)
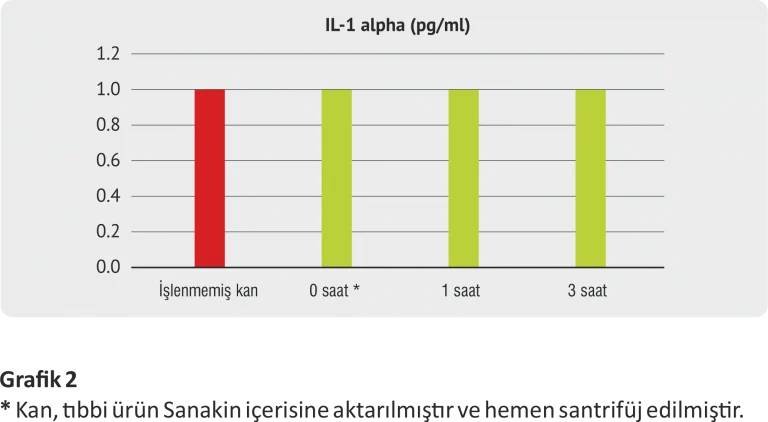
Grafiksel değerlendirme ve açıklama (Grafik 3)
İşlenmemiş kan: İnkübasyona tabii tutulmayan ve Sanakin® tıbbi cihaz kinin içine konulmamış kan, venöz kan alımında kullanılan kan alma tüpü ile hemen santrifüj edilmiştir.
• IL-1β yüksek etkili bir sitokindir, genel olarak enflamasyon mediatörleri kapsamına girmektedir.
• IL-1β etkisi Interlökin-1α ile aynıdır.
• IL-1β, İnterlökin-6’nın açığa çıkmasını tetikler.
• Bu grafikte de, her iki inkübasyon süresinde pro-inflamatuar IL-1β artışının olmadığı görülmektedir
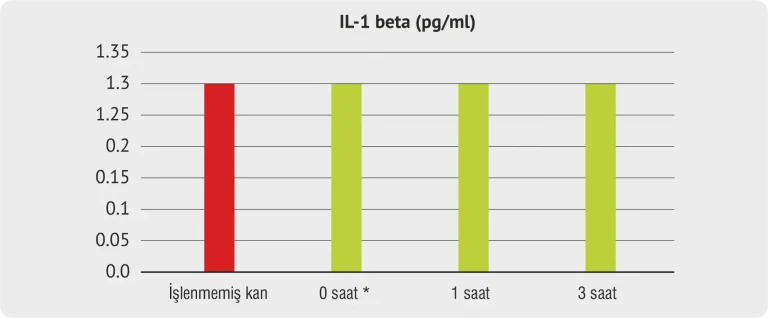
Grafik 4
* Kan, tıbbi ürün Sanakin® içerisine aktarılmıştır ve hemen santrifüj edilmiştir.
Grafiksel değerlendirme ve açıklama (Grafik 4)
İşlenmemiş kan: İnkübasyona tabii tutulmayan ve Sanakin® tıbbi cihaz kinin içine konulmamış kan, venöz kan alımında kullanılan kan alma tüpü ile hemen santrifüj edilmiştir.
• IL-6, organizmanın enflamasyon reaksiyonunu düzenleyen interlökinler kapsamına girmektedir.
• Sağlıklı kişide plazma içerisindeki IL-6 konsantrasyonu yaklaşık 1 pg/ml’dir.
• Grafik, IL-6’nın 1,5 – 2 pg/ml değerleri arasında hareket ettiğini belirgin şekilde göstermektedir. Değerlendirmede interlökinin kritik değere sahip olmadığı belirlenmiştir
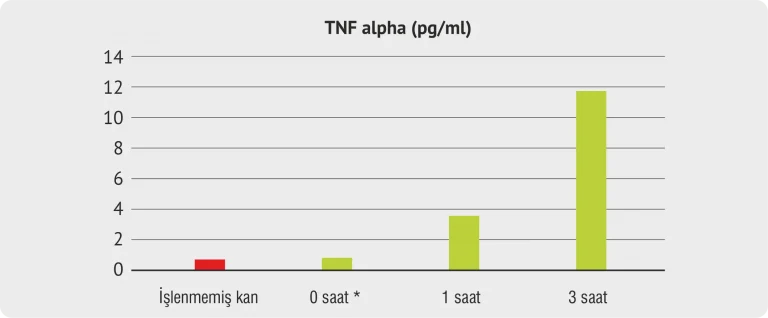
Grafik 5
* Kan, tıbbi ürün Sanakin® içerisine aktarılmışr ve hemen santrifüj edilmiştir
Grafik 5
* Kan, tıbbi ürün Sanakin® içerisine aktarılmışr ve hemen santrifüj edilmiştir
Grafiksel değerlendirme ve açıklama (Grafik 5)
İşlenmemiş kan: İnkübasyona tabii tutulmayan ve Sanakin® tıbbi cihaz kitinin içine konulmamış kan, venöz kan alımında kullanılan kan alma tüpü ile hemen santrifüj edilmiştir.
• TNF-α, bağışıklık sisteminin çok fonksiyonlu bir sitokindir. Lokal ve sistemik enflamasyona kalmaktadır.
• TNF-α’nın normal değeri 0–25 pg/ml aralığındadır, burada ölçülen değerler normal aralıktadır.

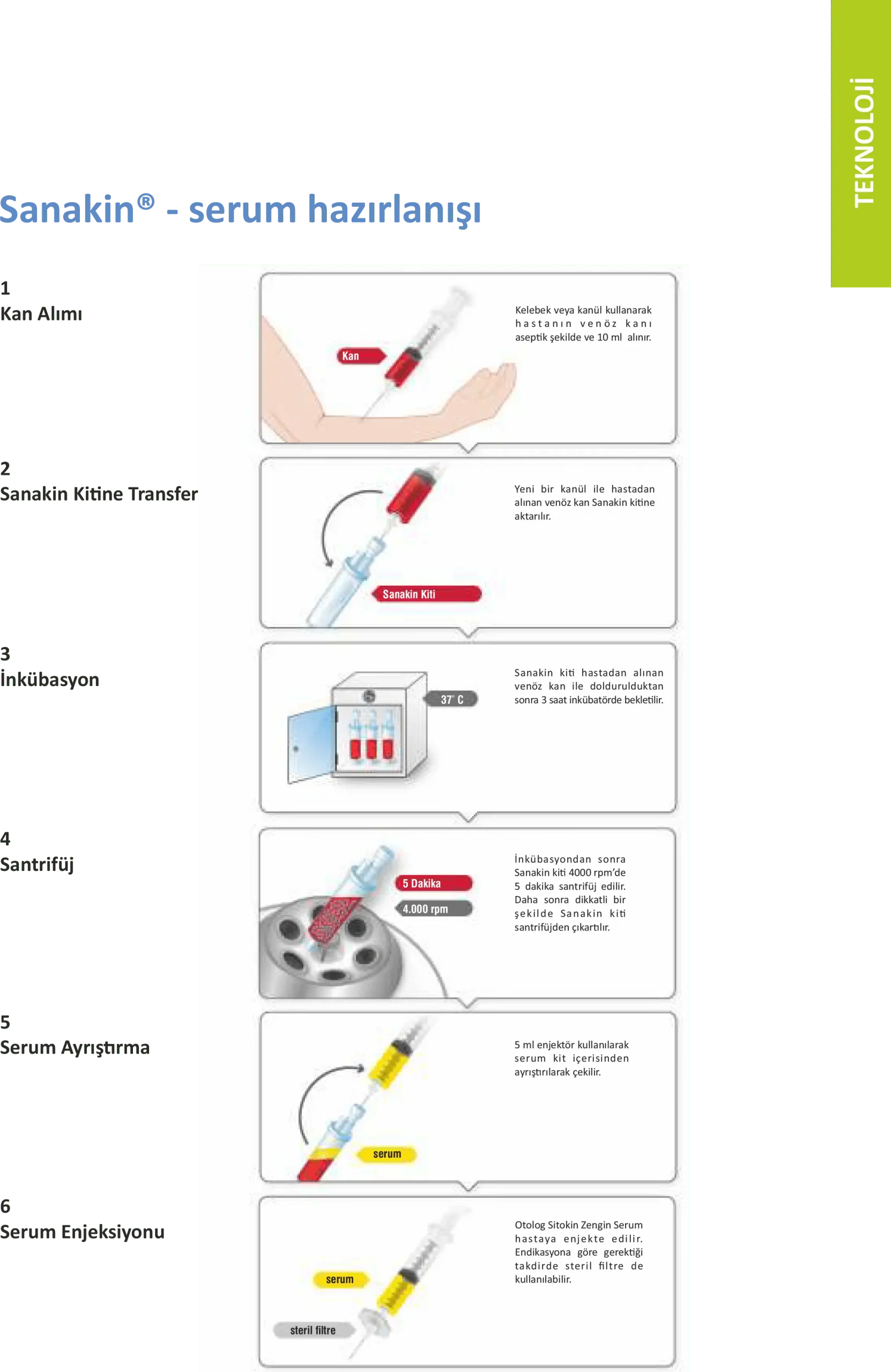
Sanakin® tıbbi ürününün kullanımı sayesinde, hastanın kanından otolog bir serum elde edilir:
ACRS ( Autologuos Cytokine Rich Serum = Otolog Sitokin Yönünden Zengin Serum).
Bu serum, inflamasyonu önleme ve doku yenilemeye yönelik yüksek konsantrasyonlu, anti-inflamatuar sitokinler ve büyüme faktörleri içerir. İşleme tabii tutulmamış doğal seruma göre, çok daha fazla miktarda anti-inflamatuar interlökin ve büyüme faktörü içeren bu serum, ihtiyaç duyulan dokuda inflamasyon karşı etki gösterir aynı zamanda doku onarımını da sağlar. Sanakin® ACRS, farklı uzmanlık alanlarında görev yapan hekimlere, endikasyona özel çözüm sunar.
